摘要
为测定白卡纸中的淀粉含量,本研究选用α-淀粉酶和糖化酶对白卡纸进行双酶协同降解,采用3,5-二硝基水杨酸(DNS)比色法对酶解产物葡萄糖进行测定,进而计算白卡纸中的淀粉含量。在单因素实验分析研究的基础上,采用响应面分析法优化双酶水解-DNS比色法测定淀粉含量的最佳条件,建立数学模型,回归方程失拟误差不显著(P<0.000 1),理论值与测定值吻合(
白卡纸具有定量高、坚挺厚实等特点,广泛应用于印刷和包装行业,卷烟行业中白卡纸每年需求量达50~60万
目前,我国还没有纸张中淀粉含量测定的相关标准。美国TAPPI T 419 om—2010提供了纸张中淀粉含量的测定方法,但该方法只适合纸张中原淀粉及仅通过常规氧化技术或酶转化改性的淀粉定量测定,不适合阳离子淀粉、取代淀粉、接枝淀粉或与树脂结合的淀粉等含量的测定。国内研究者依据淀粉遇碘会生成蓝色络合物的原理,建立了一种利用分光光度计测定纸张中淀粉含量的方
淀粉是天然存在的重要碳水化合物,广泛存在于各种植物中;同时,淀粉在食品中有着广泛的应用。研究者对植物和食品中淀粉含量的测定提出了多种方
白卡纸,湖北中烟技术中心;3,5-二硝基水杨酸(DNS)显色液,飞净生物科技有限公司;阳离子淀粉,江西六和化工实业有限公司;糖化酶(酶活性130 000 U/g),湖南鸿鹰祥生物工程股份有限公司;α-淀粉酶(酶活性4 000 U/g),北京双旋微生物培养基制品厂;葡萄糖、冰醋酸、醋酸钠、碘、碘化钾,均为分析纯,国药集团化学试剂有限公司;水为实验室自制超纯水。
准确称取5.000 0 g淀粉于500 mL烧杯中,倒入少量蒸馏水搅拌均匀,加入到正在沸腾的蒸馏水中,用蒸馏水对烧杯进行少量多次洗涤,洗涤水也加入烧杯中,继续加热沸腾5 min,冷却至室温后,用蒸馏水定容至500 mL,淀粉溶液的质量浓度为10 g/L。
称取0.5 g样品,加入100 mL pH值为4.8的醋酸-醋酸钠缓冲溶液浸泡12 h,在分散器上分散,用100 mL缓冲溶液分多次洗涤后,倒入500 mL的具塞三角烧瓶中,置于水浴恒温振荡器保温30 min后,加入糖化酶与α-淀粉酶的混合液,使溶液的总体积为300 mL。反应结束后用移液管吸取0.5 mL酶解液,加入0.5 mL DNS显色液,于沸水浴中加热5 min,取出后用流动水迅速冷却,加入4.0 mL蒸馏水,摇匀,用过滤头过滤后在540 nm波长处测定光吸收值。
在糖化酶与α-淀粉酶双酶水解白卡纸淀粉的过程中,影响淀粉水解的因素主要有双酶质量比、双酶添加量、酶解时间、酶解温度等。本研究选择双酶质量比、双酶添加量、酶解温度、酶解时间4个因素分别进行单因素实验。通过多次预实验,对各单因素条件的酶解条件进行设定,具体见
| 单因素条件 | 固定酶解条件 |
|---|---|
| 双酶质量比(8∶1、6∶1、2∶1、2∶3、1∶3) | 双酶添加量5 mg/mL,酶解温度60 ℃,酶解时间120 min,溶液体积300 mL |
| 双酶添加量(3、4、5、6、7 mg/mL) | 双酶质量比2∶1,酶解温度60 ℃,酶解时间120 min,溶液体积300 mL |
| 酶解时间(10、30、60、90、120 min) | 双酶质量比2∶1,双酶添加量5 mg/mL,酶解温度60 ℃,溶液体积300 mL |
| 酶解温度(30、40、50、60、70 ℃) | 双酶质量比2∶1,双酶添加量5 mg/mL ,酶解时间60 min,溶液体积300 mL |
白卡纸中淀粉含量由
| % | (1) |
式中,X为纸张样品中淀粉含量,%;V为酶解反应溶液的总体积,mL;0.5为DNS比色法测定所取待测液的体积,mL;m为样品的平均吸光度值代入标准曲线方程计算得出的葡萄糖含量,mg;0.9为葡萄糖与淀粉之间的换算系数;M为纸张样品质量,g。
取6支10 mL比色管并编号,按
| m=0.410 6A540 + 0.002 | (2) |
| 试管编号 | 0.5 g/L葡萄糖标准液/mL | 蒸馏水/mL | DNS试剂/mL | 葡萄糖含量/mg | A540 |
|---|---|---|---|---|---|
| 0 | 0 | 0.5 | 0.5 | 0 | 0 |
| 1 | 0.1 | 0.4 | 0.5 | 0.05 | 0.11 |
| 2 | 0.2 | 0.3 | 0.5 | 0.10 | 0.241 |
| 3 | 0.3 | 0.2 | 0.5 | 0.15 | 0.355 |
| 4 | 0.4 | 0.1 | 0.5 | 0.2 | 0.493 |
| 5 | 0.5 | 0 | 0.5 | 0.25 | 0.599 |
采用扣除空白样吸光度后,A540=0.01所对应的浓度值为检出限,此时300 mL反应液对应的葡萄糖质量浓度约为12.2 mg/L,换算为淀粉浓度约11.0 mg/L,因此纸张样品中淀粉含量的检出限为0.66%。
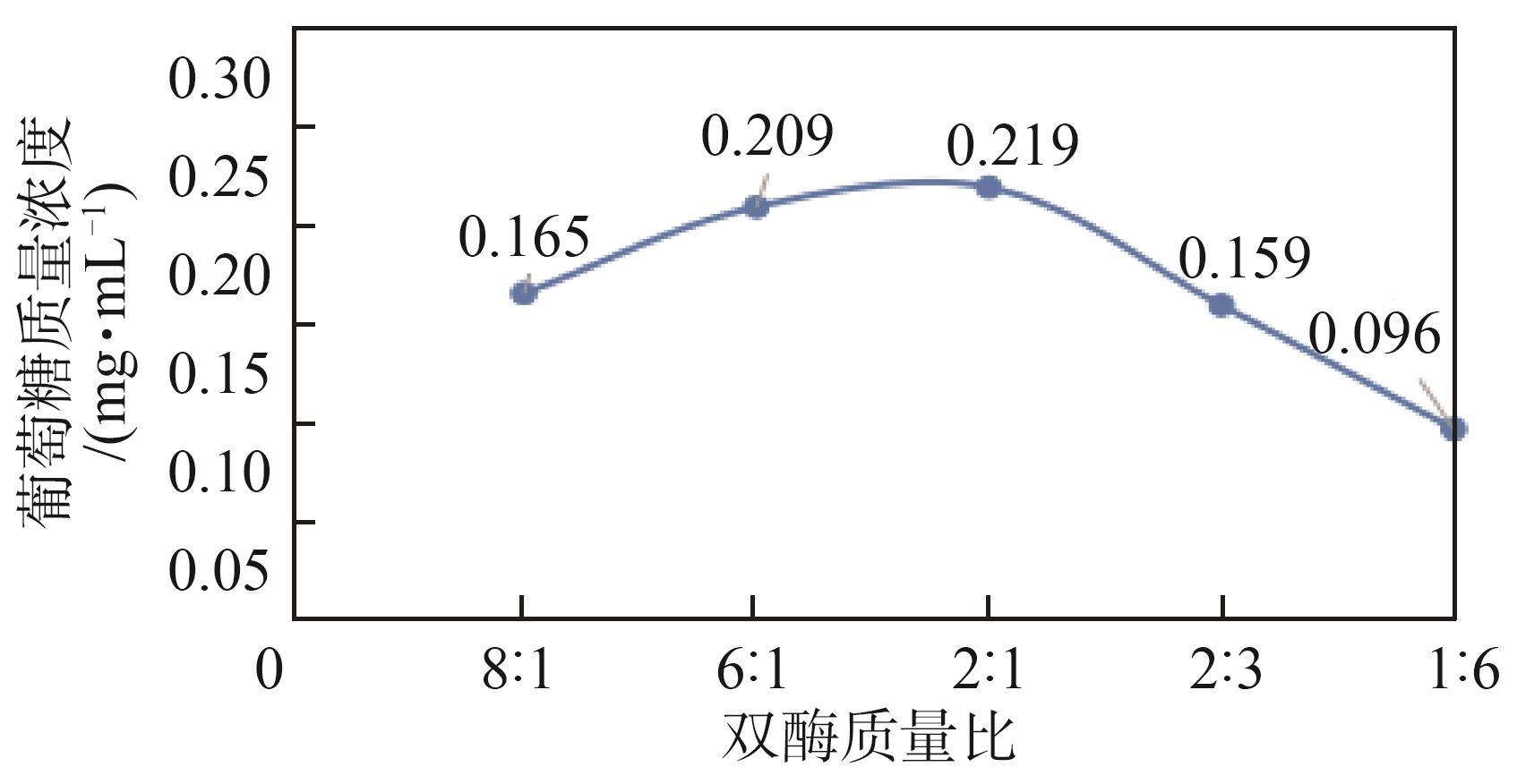
图1 双酶质量比对白卡纸中淀粉水解的影响
Fig. 1 Effect of double enzyme mass ratio on starch enzymatic hydrolysis in white cardboard
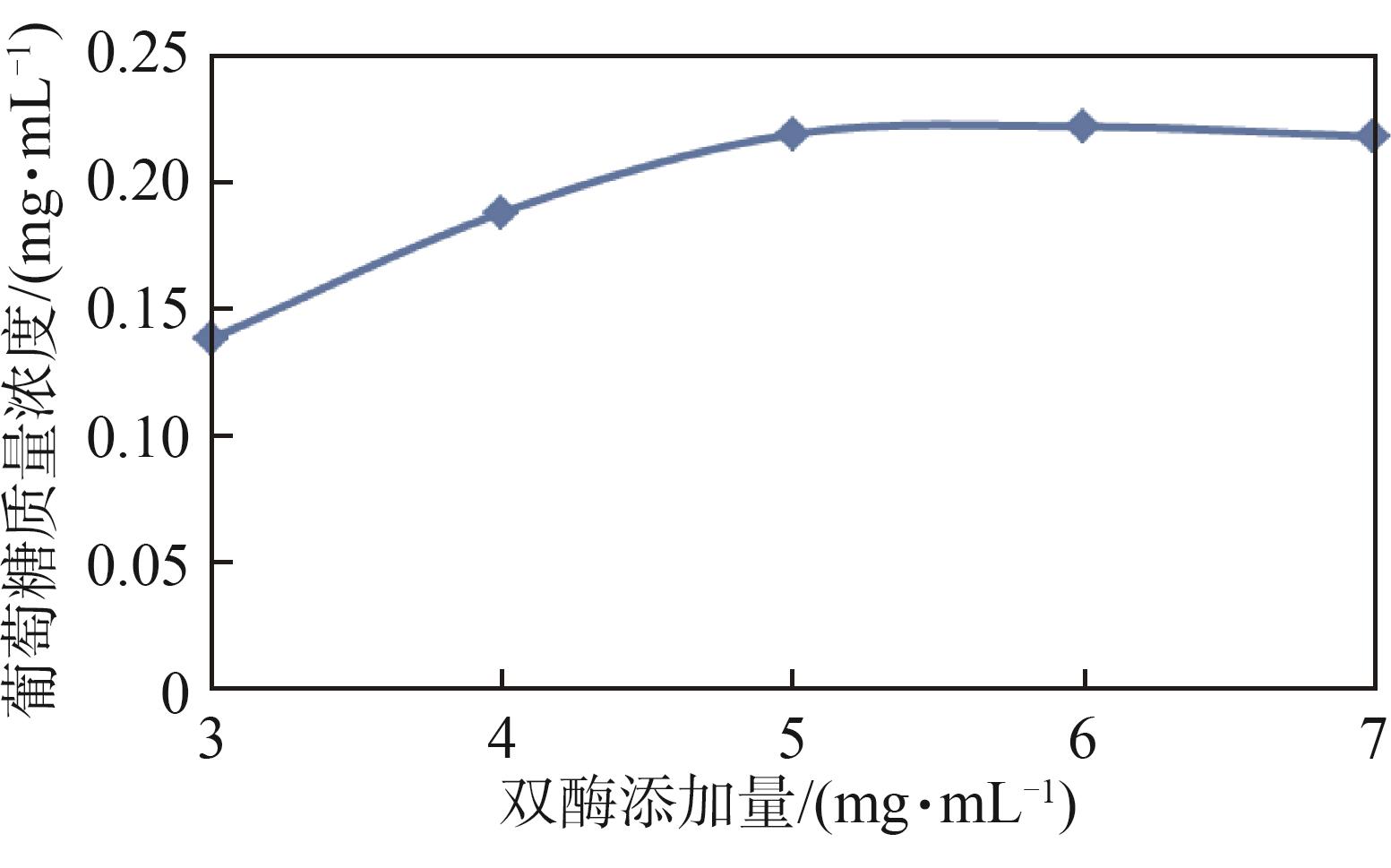
图2 双酶添加量对白卡纸中淀粉水解的影响
Fig. 2 Effect of double enzyme addition amount on starch enzymatic hydrolysis in white cardboard
根据单因素探索实验结果,以双酶添加量(X1)、酶解时间(X2)、酶解温度(X3)3个参数为自变量,葡萄糖质量浓度为响应值,设计了三因素三水平17个实验点的响应面实验,水平设计见
| 水平 | X1/(mg·m | X2/min | X3/℃ |
|---|---|---|---|
| -1 | 3 | 30 | 40 |
| 0 | 4 | 60 | 50 |
| 1 | 5 | 90 | 60 |
| 序号 | X1 | X2 | X3 | 葡萄糖质量浓度/(mg·m |
|---|---|---|---|---|
| 1 | -1 | -1 | 0 | 0.072 |
| 2 | 1 | -1 | 0 | 0.111 |
| 3 | -1 | 1 | 0 | 0.144 |
| 4 | 1 | 1 | 0 | 0.214 |
| 5 | -1 | 0 | -1 | 0.112 |
| 6 | 1 | 0 | -1 | 0.219 |
| 7 | -1 | 0 | 1 | 0.138 |
| 8 | 1 | 0 | 1 | 0.185 |
| 9 | 0 | -1 | -1 | 0.101 |
| 10 | 0 | 1 | -1 | 0.179 |
| 11 | 0 | -1 | 1 | 0.093 |
| 12 | 0 | 1 | 1 | 0.190 |
| 13 | 0 | 0 | 0 | 0.138 |
| 14 | 0 | 0 | 0 | 0.137 |
| 15 | 0 | 0 | 0 | 0.136 |
| 16 | 0 | 0 | 0 | 0.138 |
| 17 | 0 | 0 | 0 | 0.139 |
对
| Y=-0.013 2+0.006 7X1+0.056 4X2+0.000 1X3+0.001 5X1X2+0.000 9X1X3+0.000 4X2X3+0.000 6X | (3) |
对该回归方程及系数进行显著性检验,结果见
| 方差来源 | 平方和 | 自由度 | 均方 | F值 | P值 | 显著性 |
|---|---|---|---|---|---|---|
| 模型 | 0.085 6 | 9 | 0.009 5 | 67.35 | < 0.000 1 | ** |
| X1 | 0.006 7 | 1 | 0.006 7 | 47.64 | 0.000 2 | ** |
| X2 | 0.056 4 | 1 | 0.056 4 | 399.73 | < 0.000 1 | ** |
| X3 | 0.000 1 | 1 | 0.000 1 | 0.796 7 | 0.401 7 | |
| X1X2 | 0.001 5 | 1 | 0.001 5 | 10.77 | 0.013 5 | * |
| X1X3 | 0.000 9 | 1 | 0.000 9 | 6.37 | 0.039 5 | * |
| X2X3 | 0.000 4 | 1 | 0.000 4 | 2.56 | 0.153 9 | |
|
X | 0.000 6 | 1 | 0.000 6 | 4.47 | 0.072 2 | |
|
X | 0.018 8 | 1 | 0.018 8 | 132.85 | < 0.000 1 | ** |
|
X | 0.000 7 | 1 | 0.000 7 | 5.23 | 0.056 0 | |
| 残差 | 0.001 0 | 7 | 0.000 1 | |||
| 失拟误差 | 0.001 0 | 3 | 0.000 3 | |||
| 纯误差 | 0 | 4 | 0 | |||
| 总离差 | 0.086 6 | 16 |
注 **表示高度显著(P<0.01);*表示差异显著(P<0.05)。
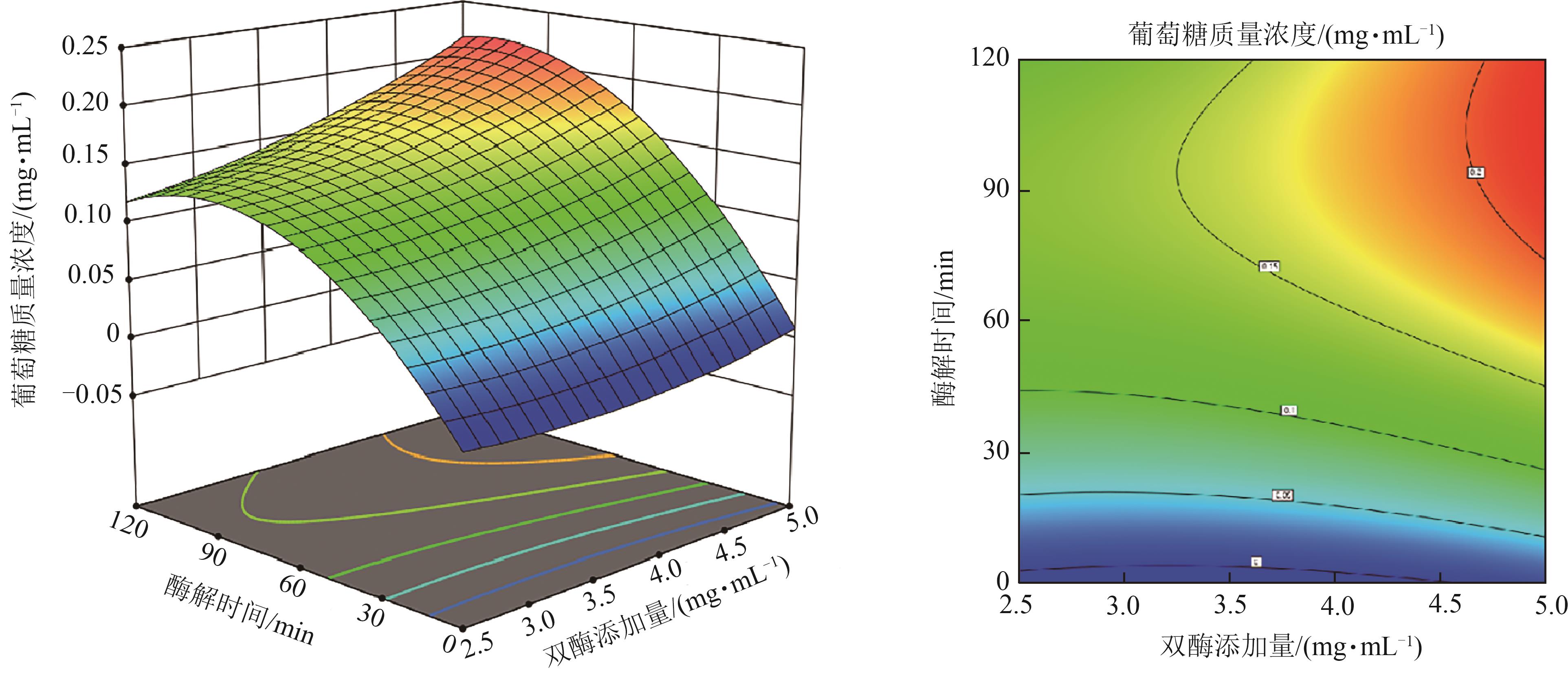
图5 酶解时间与双酶添加量对葡萄糖质量浓度的响应面和等值线
Fig. 5 Response surface plots and contour plots of the glucose mass concertration under the interaction of enzymatic hydrolysis time and double enzyme addition amount
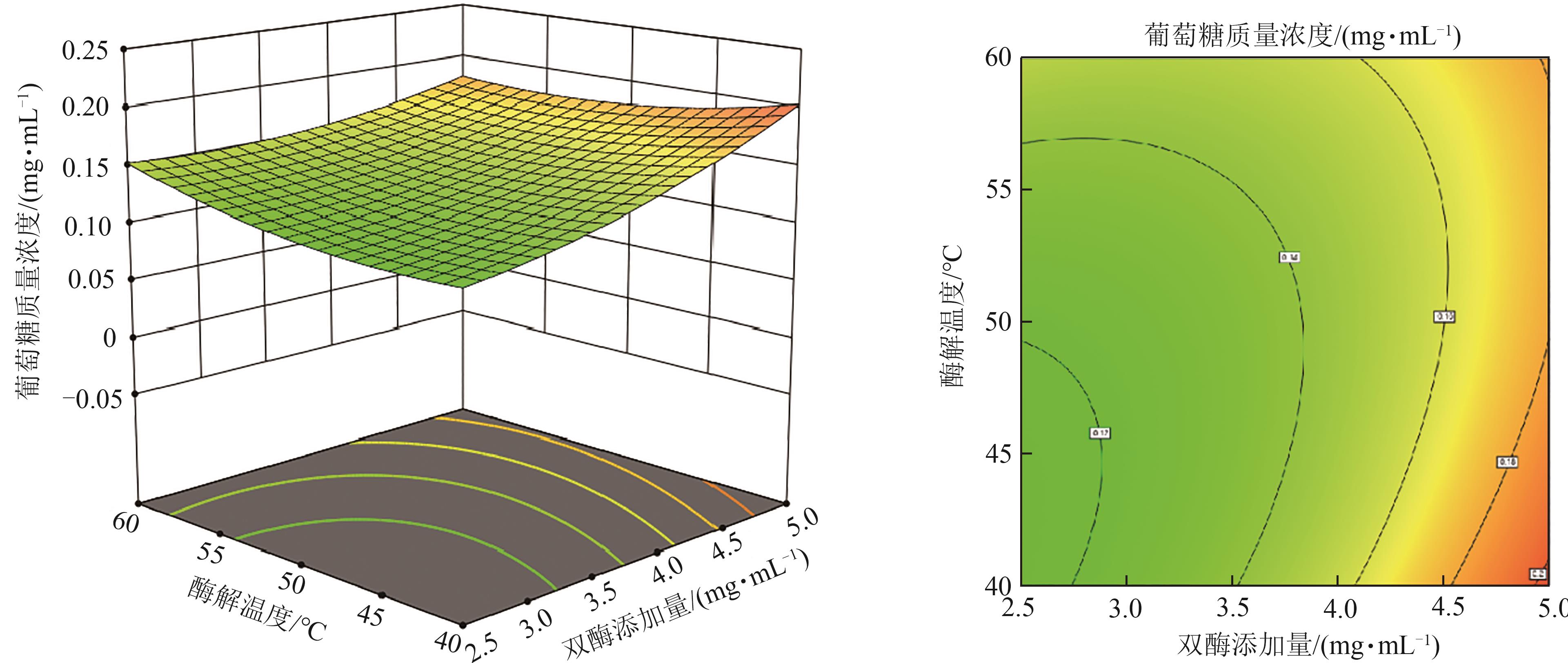
图6 酶解温度与双酶添加量对葡萄糖质量浓度的响应面和等值线
Fig. 6 Response surface plots and contour plots of the glucose mass concertration under the interaction of enzymatic temperature and double enzyme addition amount
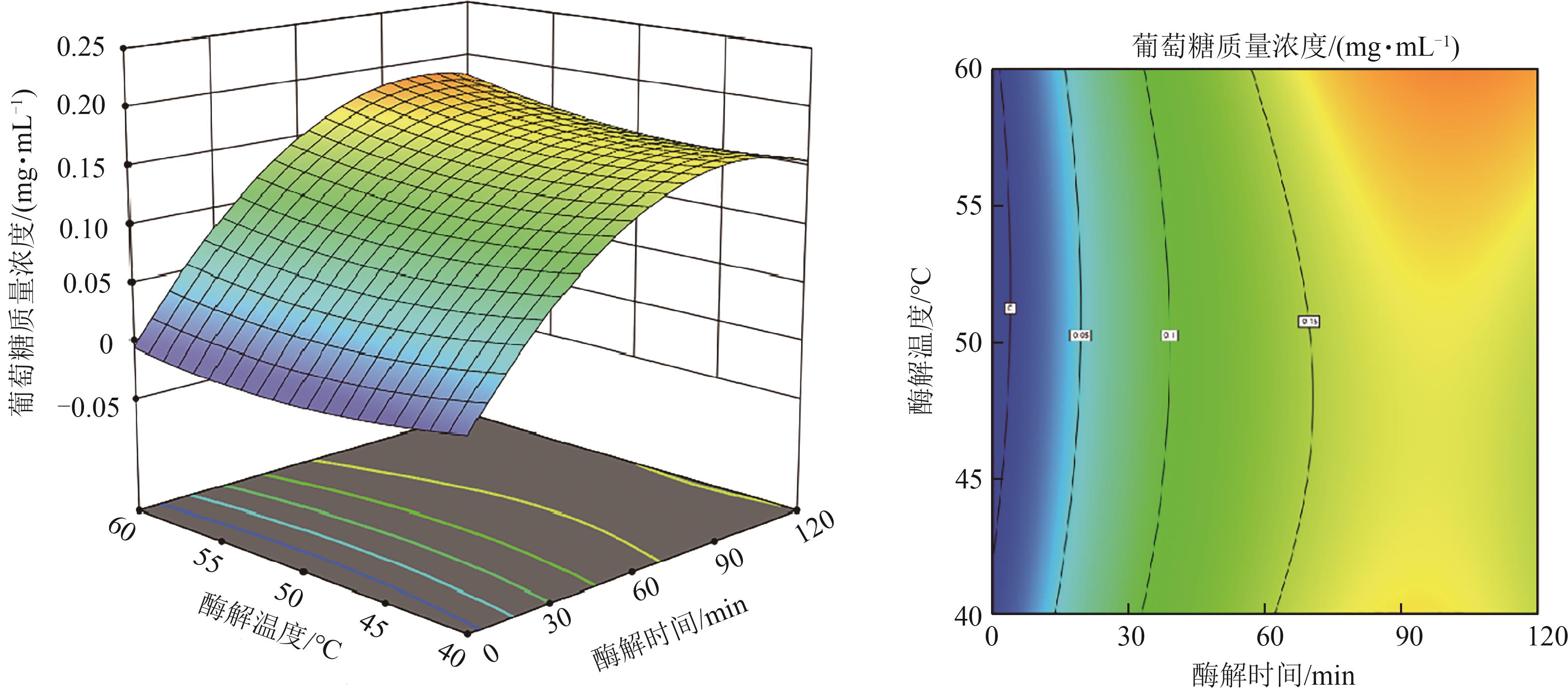
图7 酶解温度与酶解时间对葡萄糖质量浓度的响应面和等值线
Fig. 7 Response surface plots and contour plots of the glucose mass concertration under the interaction of enzymatic temperature and time
采用淀粉酶与糖化酶双酶对白卡纸中的淀粉进行水解,使其生成葡萄糖,利用3,5-二硝基水杨酸(DNS)比色法定量测定葡萄糖含量,再由葡萄糖含量计算出纸张中淀粉含量。双酶水解-DNS比色法测定淀粉含量的最佳条件为双酶添加量5 mg/mL,酶解时间75 min,酶解温度40 ℃。该方法相对标准偏差为0.8%,加标回收率为96.2%~98.0%,具有操作简单、重复性好、回收率高、测试结果准确可靠等特点,可用于白卡纸中淀粉含量的测定,也为纸和纸板中淀粉含量的测定提供新思路、新方法。
参考文献
朱红艳, 贾伟萍, 孙 鹏, 等. 烟用印刷白卡纸“返黄”机制的研究[J]. 包装工程, 2022, 43(9): 39-45. [百度学术]
ZHU H Y, JIA W P, SUN P, et al. Brightness Reversion Mechanism of White Cardboard for Tobacco Printing[J]. Packaging Engineering, 2022, 43(9): 39-45. [百度学术]
赵德清, 杨汝男, 平清伟. 烟包用涂布白卡纸国内发展概况[J]. 上海造纸, 2007, 38(1): 33-38. [百度学术]
ZHAO D Q, YANG R N, PING Q W. Survey to Coated Card Board Used as Cigarette Packing[J]. Shanghai Paper Industry, 2007, 38(1): 33-38. [百度学术]
唐少敏.阳离子直链淀粉和支链淀粉的吸附行为差异及其对纸张增强效果的影响[D].南京:南京林业大学, 2023. [百度学术]
TANG S M. Differences in adsorption behavior of cationic amylose and amylopectin and their effects on paper enhancement[D].Nanjing: Nanjing Forestry University, 2023. [百度学术]
尹沾合, 江剑芳.淀粉在涂布白卡纸中的应用研究[J].中国造纸, 2009, 28(7):46-48. [百度学术]
YIN Z H,JIANG J F.Application of Starch in Coated Ivory Board [J].China Pulp & Paper ,2009, 28(7):46-48. [百度学术]
王春林, 宋荣钊, 沈伟民, 等. 纸上淀粉含量的快速测定法[J].广州化学, 1988(3):53-56. [百度学术]
WANG C L , SONG R Z, SHEN W M, et al. Rapid Determination Method for Starch Content in Paper[J]. Guangzhou Chemical, 1988(3):53-56. [百度学术]
徐嵘, 谢堂堂, 陈桂强, 等.分光光度法测定纸品中淀粉含量[J].中国造纸, 2012, 31(2):19-22. [百度学术]
XU R, XIE T T, CHEN G Q, et al. Quantitative Determination of Starch in Paper by Spectrophotometer[J]. China Pulp&Paper, 2012, 31(2):19-22. [百度学术]
郭欣, 侯鑫, 李党国.分光光度法测试卷烟用纸中淀粉的含量[J].中华纸业, 2019, 40(16):34-37. [百度学术]
GUO X, HOU X, LI D G. Determination of Starch Content in Cigarette Paper Through Spectrophotometry[J]. China Pulp & Paper Industry, 2019, 40(16):34-37. [百度学术]
张茹.采用热解技术直接检测纸张中阳离子淀粉含量[J].国际造纸, 2015, 34(1):55-61. [百度学术]
ZHANG R. Direct Determination of Cationic Starches in Paper Samples Using Analytical Pyrolysis[J].World Pulp and Paper, 2015, 34(1):55-61. [百度学术]
李兵, 肖香兰, 杨永红,等. 国内外淀粉含量的检测标准现状及检测方法研究进展[J]. 食品安全质量检测学报, 2021, 12(9):3830-3839. [百度学术]
LI B, XIAO X L, YANG Y H, et al. Current Situation of Standard Methods and Research Progress of Starch Content Determination at China and Abroad[J]. Journal of Food Safety and Quality, 2021, 12(9):3830-3839. [百度学术]
李长滨, 崔丽伟, 庄军辉. 火腿肠中影响淀粉测定干扰项方法研究[J]. 现代牧业, 2019, 3(3): 50-51. [百度学术]
LI C B, CUI L W, ZHUANG J H. A method to determine interferences in measuring starch in ham sausage [J]. Modern Animal Husbandry, 2019, 3(3): 50-51. [百度学术]
郭有辉, 胡露, 王丽娜, 等. 3,5-二硝基水杨酸比色法测定风味鱿鱼中淀粉及蔗糖的含量[J]. 食品安全质量检测学报, 2018, 9(18):4983-4987. [百度学术]
GUO Y H, HU L, WANG L N, et al. Determination of starch and sucrose in flavor squid by 3,5-dinitrosalicylic acid colorimetric method [J]. Journal of Food Safety and Quality, 2018, 9(18): 4983-4987. [百度学术]
蔡志兴. 肉松制品淀粉含量测定中干扰物质的研究[J]. 福建分析测试, 2013, 22(6): 49-52. [百度学术]
CAI Z X. Study of the Interfering Substances in the Dried Meat Floss Starch Content Determination[J]. Fujian Analysis Testing, 2013, 22(6): 49-52. [百度学术]
方勇, 赵胜军, 张丹丹, 等. 饲料纤维水平对其淀粉含量测定方法准确性的影响[J]. 粮食与饲料工业, 2015(8): 66-68. [百度学术]
FANG Y, ZHAO S J, ZHANG D D, et al. Effect of Cellulose Level on the Accuracy of the Determination Method of Starch Content in Feed[J]. Cereal & Feed Industry, 2015(8): 66-68. [百度学术]
何孟杭. 双酶水解-高效液相色谱法测定肉松中淀粉含量的研究[J]. 福建分析测试, 2013, 22(5): 59-62. [百度学术]
HE M H. Determination of Starch in Dried Meat Floss by Double Enzymolysis-HPLC Method[J]. Fujian Analysis Testing, 2013, 22(5): 59-62. [百度学术]
李彦莹, 朱新焰, 石亚娜, 等. 酶水解法测定滇黄精淀粉含量的工艺优化[J]. 西南农业学报, 2018, 31(12): 2533-2536. [百度学术]
LI Y Y, ZHU X Y, SHI Y N, et al. Optimization Technologies of Enzymatic Hydrolysis for Determination of Starch in Polygonatum Kingianum[J]. Southwest China Journal of Agricultural Sciences, 2018, 31(12): 2533-2536. [百度学术]
徐靖雯, 郑明珠, 刘景圣, 等.复合酶法改性淀粉的研究进展[J].食品研究与开发, 2024, 45(1):187-192. [百度学术]
XU J W, ZHENG M Z, LIU J S, et al. Research Progress of Starch Modified by Compound Enzymes[J]. Food Research and Development, 2024, 45(1):187-192. [百度学术]
朱凯杰, 陆国权, 张迟. 响应面法优化水杨酸比色测定还原糖的研究[J]. 中国粮油学报, 2013, 28(8): 107-113. [百度学术]
ZHU K J, LU G Q, ZHANG C. Optimization of Salicylic Acid Colorimetric Determination of Reducing Sugar by Response Surface Methodology[J]. Journal of the Chinese Cereals and Oils Association, 2013, 28(8): 107-113. [百度学术]
李志霞, 聂继云, 闫 震, 等.响应面法对 3,5-二硝基水杨酸比色法测定水果中还原糖含量条件的优化[J].分析测试学报, 2016, 35(10):1283-1288. [百度学术]
LI Z X, NIE J Y, YAN Z, et al.Optimization of 3,5-dinitrosalicylic Acid Colorimetry Determination Conditions of Reducing Sugar in Fruits by Response Surface Method[J]. Journal of Instrumental Analysis, 2016, 35(10):1283-1288. [百度学术]

