摘要
本研究开发了一种采用定量环在线稀释-离子色谱法检测造纸法烟草薄片中L
造纸法烟草薄
烟草薄片应用于卷烟配方在国外已有60多年的历史。我国烟草薄片的工业化研究与开发始于20世纪90年代后期。源于烟草的烟草薄片,与天然烟叶有较大差别。近年来,烟草薄片技术取得了长足发展,成为了卷烟配方不可或缺的重要原料组成部分。
国家标准样品N
ICS-5000离子色谱仪(美国ThermoFisher公司,配置电导检测器);IonPac CS12A 阳离子分析及保护柱(4 mm×250 mm)(美国ThermoFisher公司);G204 电子天平(感量:0.0001 g,瑞士METTLER TOLEDO 公司);Milli-Q超纯水器(美国Millipore公司);振荡器(HY-8 调速振荡器,常州国华电器有限公司);定量加液器(德国Brand 公司);移液枪(德国Tripette公司);0.45 μm尼龙66滤膜(天津市津腾实验设备有限公司)。
取0.1 g烟草薄片(云南中烟工业有限责任公司技术中心提供)于容器中,加入50 mL 0.01 mol/L盐酸水溶液萃取剂,振荡萃取30 min后,通过0.45 μm尼龙66滤膜过滤,收集过滤后的萃取剂作为样品,置于非玻璃材质的色谱瓶中,待检测。
流动相A为 0.1 mol/L MSA淋洗液;流动相B为水;流速为1.0 mL/min。洗脱条件:等度洗脱,MSA淋洗液浓度为20.0 mmol/L;抑制器电流为59 mA;采集时间15 min。柱箱温度30 ℃,检测池温度35 ℃。进样方式:采用控温进样器,进样盘温度4 ℃。100 μL定量环的部分进样模式(PushSeqPartial);进样量25 μL;当试样中目标组分的浓度超出标准曲线范围时,在部分进样模式下,设置进样量为5 μL,实现定量环在线稀释。
对系列标准工作溶液进行色谱测定,使用保留时间定性,外标法定量。根据所配标准溶液的浓度及其响应峰面积,建立NH的二次拟合标准工作曲
| (1) |
式中,Ci为单位质量待测烟草薄片中阳离子i的质量,mg/g;为IC测定所得阳离子i的含量,μg/mL;V为萃取溶剂体积,mL;M为进行本次分析的烟草薄片的质量,g。
取2个平行样品的算术平均值为检测结果,结果精确到0.01 mg/g。平行测定结果之间的相对平均偏差(RAD)≤10%。即得到待测烟草薄片中6种阳离子的含量。
用0.05 mol/L盐酸水溶液作萃取剂,采用不同材质的试剂瓶,玻璃试剂瓶和可溶性聚四氟乙烯(PFA)试剂瓶,分别配制、摇匀后,通过色谱法检测N
用0.05 mol/L盐酸水溶液作萃取剂,采用不同材质的三角瓶作为样品前处理容器,分别配制浓度为2.0 μg/mL的N
| 序号 | N | ||
|---|---|---|---|
| 玻璃 | 聚乙烯 | 聚四氟乙烯 | |
| 1 | 1.803 | 1.556 | 1.541 |
| 2 | 1.820 | 1.576 | 1.588 |
| 3 | 1.789 | 1.580 | 1.551 |
| 4 | 1.798 | 1.569 | 1.578 |
| 5 | 1.812 | 1.548 | 1.548 |
| 6 | 1.804 | 1.562 | 1.528 |
| 7 | 1.798 | 1.489 | 1.569 |
| 8 | 1.986 | 1.564 | 1.501 |
| 9 | 1.808 | 1.559 | 1.560 |
| 10 | 1.786 | 1.421 | 1.559 |
| 平均值 | 1.8205 | 1.5423 | 1.5523 |
| 方差 | 0.0035 | 0.0025 | 0.0006 |
| 统计检验 | 玻璃 | 聚乙烯 | 聚四氟乙烯 |
|---|---|---|---|
| F检验 | 基准 | PF=0.3066>0.05,同方差 | PF=0.0009<0.05,异方差 |
| t检验 | 基准 |
t=-11.3990,Pt=5.71×1 |
t=-13.2132,Pt=8.21×1 |
| 结论 | Pt<0.05,有显著性差异 | Pt<0.05,有显著性差异 |
基于上述利用不同材质三角瓶进行样品前处理实验结果,综合考虑到聚乙烯三角瓶单价低于玻璃和聚四氟乙烯三角瓶,因此选择聚乙烯三角瓶作为样品前处理容器。
用0.05 mol/L盐酸水溶液作萃取剂,采用玻璃容量瓶和PMP塑料容量瓶,分别配制浓度为10 μg/mL的N
| 级别 | ||||||
|---|---|---|---|---|---|---|
|
浓度/μg·m | 0.1 | 0.2 | 0.5 | 1.0 | 2.0 | 5.0 |
| 材质 | 线性方程 | 相关系数 |
|---|---|---|
| 玻璃 | Y=0.1032X+0.0156 | 0.7124 |
| PMP塑料 | Y=0.1045X+0.0427 | 0.9991 |
选用5种离子色谱仪常用萃取剂(水、1%甲酸水溶液、1%乙酸水溶液、0.05 mol/L盐酸水溶液、0.05 mol/L硫酸水溶液)作为备选萃取剂。移取上述萃取剂各50 mL于不同的聚乙烯三角瓶中,分别加入0.1 g烟草薄片,振荡萃取40 min,实验结果见
| 萃取剂 | 含量/μg· | |||||
|---|---|---|---|---|---|---|
| L | N | NH | M | C | ||
| 水 |
0.22×1 | 0.32 | 0.58 | 20.62 | 2.14 | 30.31 |
| 1%甲酸水溶液 |
0.33×1 | 0.37 | 0.66 | 23.35 | 2.65 | 35.22 |
| 1%乙酸水溶液 |
0.36×1 | 0.38 | 0.71 | 23.62 | 2.72 | 35.56 |
| 0.05 mol/L盐酸水溶液 |
0.48×1 | 0.41 | 0.77 | 24.86 | 4.19 | 42.87 |
| 0.05 mol/L硫酸水溶液 |
0.47×1 | 0.40 | 0.78 | 24.81 | 4.11 | 42.63 |
移取 6种阳离子混合标准溶液0.5 mL,分别加入100 mL不同浓度的盐酸水溶液(0.0025、0.005、0.0100、0.0200、0.0500 mol/L)稀释,稀释后浓度为L
| 萃取剂浓度/mol· | 峰面积/μS·min | 理论塔板数 | ||||||
|---|---|---|---|---|---|---|---|---|
| L | N | NH | M | C | NH | |||
| 0.0025 | 0.0738 | 0.2515 | 0.4603 | 0.1624 | 0.4366 | 1.5023 | 3248 | |
| 0.0050 | 0.0742 | 0.2534 | 0.4615 | 0.1631 | 0.4375 | 1.5027 | 3256 | |
| 0.0100 | 0.0755 | 0.2542 | 0.4631 | 0.1663 | 0.4387 | 1.5056 | 3267 | |
| 0.0200 | 0.0761 | 0.2554 | 0.4639 | 0.1675 | 0.4395 | 1.5069 | 2584 | |
| 0.0500 | 0.0769 | 0.2559 | 0.4657 | 0.1681 | 0.4397 | 1.5075 | 2567 | |
室温下,对同一烟草薄片样品分别超声萃取和振荡萃取处理,再进行色谱分析;结果表明,2种萃取方式结果相近。考虑到超声波发生器通常因不具备冷却功能导致控温精度不足,萃取过程中,超声波发生器腔体内水温会随超声时间的增长而升高,可能会影响样品中氨的含量。因此,优选振荡萃取。
对同一烟草薄片样品进行振荡萃取,分别考察10、20、30、40、50 min的萃取效率,结果见
萃取时间 /min | 含量/μg· | |||||
|---|---|---|---|---|---|---|
| L | N | NH | M | C | ||
| 10 |
0.21×1 | 0.28 | 0.39 | 15.36 | 2.52 | 22.58 |
| 20 |
0.34×1 | 0.35 | 0.60 | 21.28 | 3.67 | 32.74 |
| 30 |
0.47×1 | 0.41 | 0.79 | 24.84 | 4.18 | 42.93 |
| 40 |
0.48×1 | 0.42 | 0.78 | 24.85 | 4.19 | 42.86 |
| 50 |
0.48×1 | 0.41 | 0.78 | 24.80 | 4.16 | 42.63 |
烟草薄片中6种阳离子含量的色谱图见
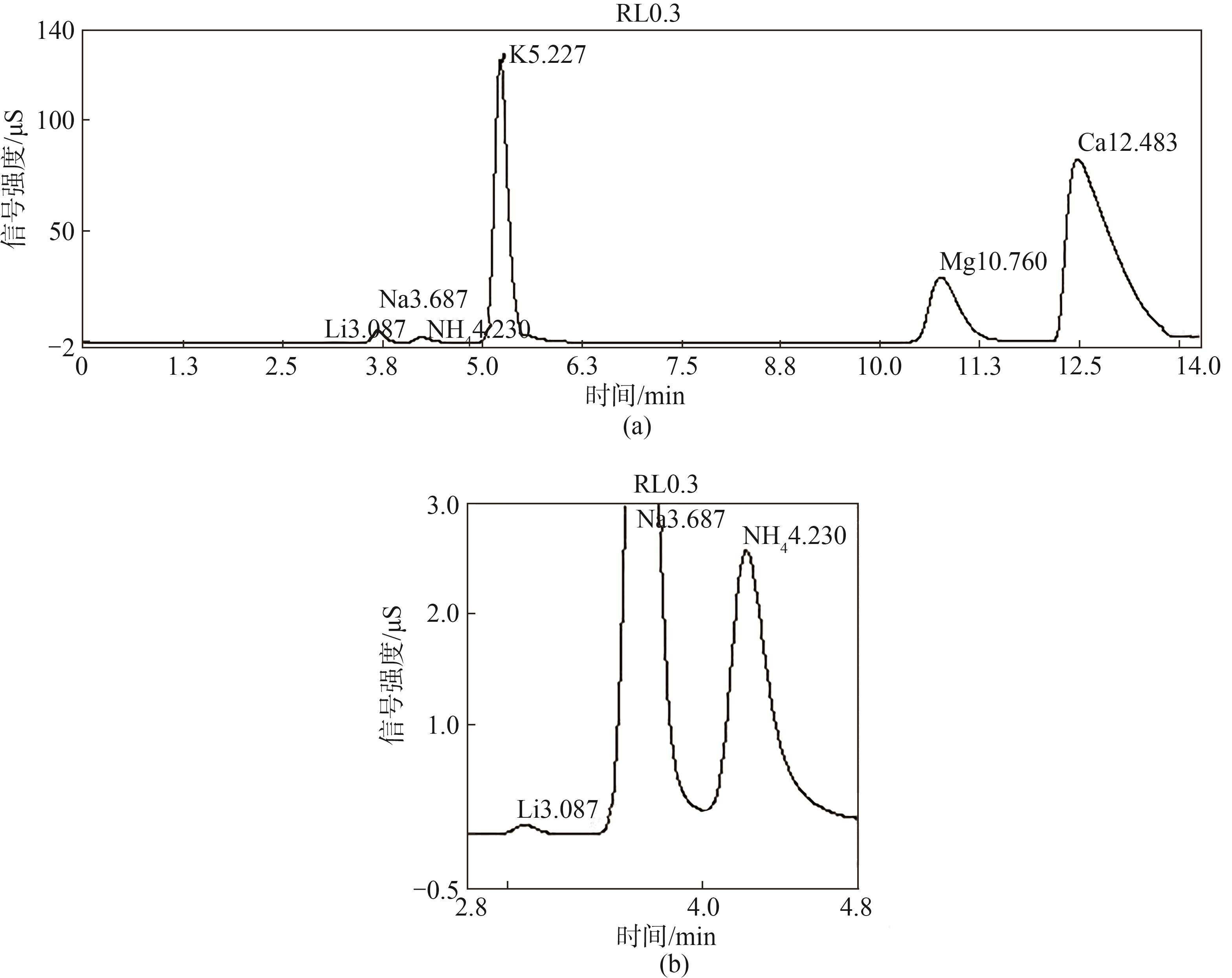
图1 烟草薄片中L
Fig.1 Ion chromatography results of L
注 图1(b)为图1(a)的局部放大图。
移取6种阳离子混合标准溶液0.5 mL置于10 mL的PMP塑料容量瓶内,用0.01 mol/L盐酸水溶液萃取剂定容,得到阳离子混合储备液(浓度分别为L
| 级别 | 浓度/μg·m | |||||
|---|---|---|---|---|---|---|
| L | N | NH | M | C | ||
|
| 0.0125 | 0.05 | 0.1 | 0.05 | 0.05 | 0.25 |
|
| 0.0250 | 0.10 | 0.2 | 0.10 | 0.10 | 0.50 |
|
| 0.0500 | 0.20 | 0.4 | 0.20 | 0.20 | 1.00 |
|
| 0.1250 | 0.50 | 1.0 | 0.50 | 0.50 | 2.50 |
|
| 0.250 | 1.00 | 2.0 | 1.00 | 1.00 | 5.00 |
|
| 0.500 | 2.00 | 4.0 | 2.00 | 2.00 | 10.00 |
|
| 1.250 | 5.00 | 10.0 | 5.00 | 5.00 | 25.00 |
|
| 2.500 | 10.00 | 20.0 | 10.00 | 10.00 | 50.00 |
在相同的检测条件下分析、测定相应标准工作溶液,以标准工作溶液浓度(μg/mL)为横坐标,分别以6种阳离子色谱峰响应值即离子峰面积(μS·min)为纵坐标,得到离子的标准线性方程(见
| 阳离子 | 线性方程 | 线性范围/μg·m | 检出限/μg·m | 定量限/μg·m | |
|---|---|---|---|---|---|
|
L | Y=1.6410X+0.05 | 0.9984 | 0.0125~2.5 | 0.014 | 0.052 |
|
N | Y=0.5188X+0.0618 | 0.9992 | 0.05~10 | 0.011 | 0.034 |
| NH |
Y=-0.0268 | 0.9988 | 0.1~20 | 0.013 | 0.045 |
|
| Y=0.3238X+0.048 | 0.9991 | 0.05~10 | 0.023 | 0.070 |
|
M | Y=0.9779X+0.1569 | 0.9994 | 0.05~10 | 0.031 | 0.094 |
|
C | Y=0.6187X+0.586 | 0.9987 | 0.25~50 | 0.028 | 0.083 |
取最低浓度标准溶液,连续测定10次,计算平行测定值的标准偏差(SD),3SD为检出限(LOD),10SD为定量限(LOQ),结果见
对同一烟草薄片按上述方法进行样品处理并进行含量测定,评价样品的重复性与重现性。日内重复性,是以同一样品每天重复测定5次,连续测定3天,计算相对标准偏差(RSD)来表示。日间重现性,是以每天测定5个不同样品,连续测定3天,计算RSD来表示,实验结果见
| 阳离子 | 日内重复性 | 日间重现性 | |||
|---|---|---|---|---|---|
| 平均值/mg· | RSD/% | 平均值/mg· | RSD/% | ||
|
L |
0.42×1 | 3.86 |
0.45×1 | 4.52 | |
|
N | 0.45 | 3.54 | 0.46 | 4.17 | |
| NH | 0.79 | 2.62 | 0.77 | 3.85 | |
|
| 24.48 | 2.36 | 24.57 | 2.87 | |
|
M | 4.57 | 3.26 | 4.59 | 3.88 | |
|
C | 43.25 | 2.14 | 43.37 | 2.57 | |
取已知阳离子含量的烟草薄片,准确称取4份,装入三角瓶内。其中3份分别按照低、中、高3种浓度水平加入阳离子混合储备液。未加标样品和3份加标后的样品分别按上述前处理方法处理样品,分别加入50 mL 0.01 mol/L盐酸水溶液,振荡萃取30 min后过滤,每个添加水平重复测定5次。在相同色谱条件进行样品分析,由原含量、加标量及测定量,计算平均回收率及加标后测定值的平均相对标准偏差(RSD)(见
| 阳离子 | 原含量/mg· | 低浓度 | 中浓度 | 高浓度 | |||||
|---|---|---|---|---|---|---|---|---|---|
回收率 /% | RSD /% | 回收率 /% | RSD /% | 回收率/% | RSD /% | ||||
|
L |
0.43×1 | 97.5 | 4.51 | 96.9 | 4.27 | 97.5 | 3.69 | ||
|
N | 0.46 | 105.9 | 4.32 | 97.4 | 2.73 | 95.8 | 1.53 | ||
| NH | 0.81 | 103.2 | 3.26 | 103.4 | 2.17 | 104.3 | 2.58 | ||
|
| 24.52 | 107.3 | 2.65 | 97.3 | 2.66 | 97.5 | 1.57 | ||
|
M | 4.53 | 98.2 | 2.76 | 97.8 | 2.93 | 98.9 | 2.48 | ||
|
C | 43.36 | 99.7 | 2.96 | 103.5 | 1.93 | 103.7 | 2.18 | ||
当样品中待测物浓度超过标准工作溶液的线性范围时,常用方式为采用萃取剂对试液进行等比例稀释,但对于NH
采用成倍增加萃取剂用量的方法对样品再次进行制备时,由于重新制备样品稀释液会耗时费工,且等待一批次样品检测完成数据分析后,原有萃取剂可能已失效。
本方法采用100 μL定量环,选用部分进样模式(PushSeqPartial),设置进样量为25 μL。当试样中目标组分的浓度超出标准曲线范围时,在部分进样模式下,设置进样量为5 μL,实现样品的在线稀释。
移取6种阳离子混合标准溶液0.5 mL,用100 mL 0.01 mol/L盐酸水溶液稀释,得到浓度为L
| 序号 | L | N | NH含量/μg·m | M | C | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 稀释a | 稀释b | 稀释a | 稀释b | 稀释a | 稀释b | 稀释a | 稀释b | 稀释a | 稀释b | 稀释a | 稀释b | ||||||
| 1 | 0.0528 | 0.0532 | 0.2077 | 0.2376 | 0.4045 | 0.3785 | 0.1918 | 0.2319 | 0.2032 | 0.2316 | 1.0321 | 0.9776 | |||||
| 2 | 0.0521 | 0.0566 | 0.1926 | 0.2225 | 0.3969 | 0.4121 | 0.1954 | 0.2212 | 0.1968 | 0.2225 | 0.9976 | 0.9885 | |||||
| 3 | 0.0486 | 0.0421 | 0.2093 | 0.2179 | 0.3953 | 0.3692 | 0.2038 | 0.2408 | 0.2026 | 0.2309 | 0.9923 | 0.9881 | |||||
| 4 | 0.0477 | 0.0466 | 0.2091 | 0.2214 | 0.4058 | 0.4414 | 0.2066 | 0.2315 | 0.2045 | 0.2214 | 0.9911 | 1.0618 | |||||
| 5 | 0.0525 | 0.0439 | 0.1922 | 0.1807 | 0.3915 | 0.3788 | 0.2082 | 0.1887 | 0.2058 | 0.1780 | 0.9942 | 1.0938 | |||||
| 平均值 | 0.0507 | 0.0485 | 0.2022 | 0.2160 | 0.3988 | 0.3960 | 0.2012 | 0.2228 | 0.2026 | 0.2169 | 1.0015 | 1.0220 | |||||
| SD/% | 0.21 | 0.55 | 0.80 | 1.89 | 0.55 | 2.70 | 0.64 | 1.82 | 0.31 | 1.99 | 1.55 | 4.69 | |||||
| RSD/% | 4.23 | 11.43 | 3.96 | 8.75 | 1.38 | 6.81 | 3.20 | 8.15 | 1.53 | 9.17 | 1.55 | 4.59 | |||||
| Pt | 0.4686,无显著性差异 | 0.2146,无显著性差异 | 0.8439,无显著性差异 | 0.0546,无显著性差异 | 0.1930,无显著性差异 | 0.4302,无显著性差异 | |||||||||||
注 稀释a为定量环在线稀释;稀释b为人工稀释。
| 序号 | 含量/μg· | |||||
|---|---|---|---|---|---|---|
| L | N | NH | M | C | ||
| 样品1 |
0.81×1 | 1.16 | 1.05 | 16.23 | 2.63 | 41.78 |
| 样品2 | — | 0.36 | 1.27 | 5.13 | 3.52 | 31.64 |
| 样品3 | — | 0.48 | 0.64 | 15.03 | 2.57 | 37.33 |
| 样品4 | — | 0.72 | 0.59 | 21.37 | 6.24 | 42.37 |
| 样品5 | — | 0.59 | 0.84 | 18.32 | 3.94 | 35.28 |
| 样品6 | — | 1.02 | 1.14 | 12.38 | 3.26 | 36.37 |
| 样品7 |
0.27×1 | 1.27 | 1.31 | 15.22 | 3.57 | 48.71 |
| 样品8 | — | 0.64 | 0.62 | 22.58 | 4.25 | 34.68 |
本研究开发了一种样品前处理简单快捷、试剂用量少、环境污染小、检测成本低的方法,使用离子色谱法检测造纸法烟草薄片中L
3.1 在0.1 g样品用50 mL 0.01 mol/L盐酸水溶液室温振荡萃取30 min的条件下,上述6种阳离子的检出限、定量限分别可达0.011~0.031 μg/mL、0.034~0.094 μg/mL,线性相关系数达0.998以上;日内重复性和日间重现性分别2.14%~3.86%、2.57%~4.52%,表明该方法重复性与重现性较好;在3种不同添加浓度下,6种阳离子的加标回收率均在95.8%~107.3%之间,相对标准偏差(RSD)均在1.53%~4.51%之间。
3.2 采用定量环在线稀释方式,方便快捷,适用于大通量检测,且检测结果准确度明显由于人工稀释方式,精密度较好,相较于人工稀释方式,精密度提高了1倍以上。经检验,不同造纸法烟草薄片样品中所含阳离子的种类存在差异,且含量差异较大。
参考文献
祁 凯,董继先,刘 欢,等.造纸法烟草薄片磨浆专用磨片的研究与应用[J].中国造纸,2021,40(1):55-61. [百度学术]
QI K, DONG J X, LIU H, et al. Research and Application of Special Refining Plates for Reconstituted Tobacco Sheet[J]. China Pulp & Paper, 2021,40(1):55-61. [百度学术]
刘良才,李炳堂,许国齐,等.造纸法烟草薄片废水碳源回收研究[J].纸和造纸,2019,38(5):41-46. [百度学术]
LIU L C, LI B T, XU G Q, et al. Research on Carbon Source Recovery of Wastewater from Paper-making Reconstituted Tobacco Sheet[J]. Paper and Paper Making,2019,38(5):41-46. [百度学术]
喻世涛,程 璇,姚建武,等.加热非燃烧烟草薄片热导性能的提升研究[J].中国造纸,2022,41(7):60-66. [百度学术]
YU S T, CHENG X, YAO J W, et al. Study on Improving Thermal Conductivity of Non-combustion Tobacco Sheet[J]. China Pulp & Paper, 2022,41(7):60-66. [百度学术]
李国政,周 浩,陈芝飞,等.造纸法再造烟叶主要工艺过程中的阳离子含量[J].烟草科技,2017,50(6):47-52. [百度学术]
LI G Z, ZHOU H, CHEN Z F, et al. Cation content during paper-making tobacco reconstitution processes[J]. Tobacco Science & Technology, 2017,50(6):47-52. [百度学术]
宋顺喜,吴泽仕,张美云,等.烟梗颗粒加填对再造烟叶基片物理性能的影响[J].中国造纸,2020,39(10):44-49. [百度学术]
SONG S X, WU Z S, ZHANG M Y, et al. Effect of Tobacco Stem Particles Filling on the Physical Properties of Reconstituted Tobacco Sheets[J]. China Pulp & Paper, 2020,39(10):44-49. [百度学术]
YC/T 16.3—2003. 再造烟叶 第3部分:造纸法[S]. [百度学术]
YC/T16.3—2003. Reconstituted Tobacco-Part 3: paper processes[S]. [百度学术]
李国政,张峻松,邱建华,等. 离子色谱法测定再造烟叶中的钠·氨·钾·镁·钙[J].安徽农业科学,2014,42(2):575-576,635. [百度学术]
LI G Z, ZHANG J S, QIU J H, et al. Determination of N
汤建国,黄燕南,伊奥尔,等.离子色谱法测定造纸法再造烟叶中几种阳离子含量[J].中国造纸,2013,32(5):31-35. [百度学术]
TANG J G, HUANG Y N, YI A E, et al. Determination of Cations in Reconstituted Tobacco by Using Ion Chromatography[J]. China Pulp & Paper, 2013,32(5):31-35. [百度学术]
张 健,李 超,陶 鹰,等.离子色谱研究深度抽吸模式下卷烟主流烟气中氨的逐口释放量[J].云南农业大学学报(自然科学版),2016,31(5):856-861. [百度学术]
ZHANG J, LI C, TAO Y, et al. Study of Ammonia Release in Mainstream Cigarette Smoke under Intensive Smoking Regime by Ion Chromatography[J]. Journal of Yunnan Agricultural University (Natural Science Edition),2016,31(5):856-861. [百度学术]
秦亚琼,王晓瑜,贾云祯,等. 无烟气烟草制品化学成分研究进展[J]. 烟草科技,2018,51(2):95-106. [百度学术]
QIN Y Q, WANG X Y, JIA Y Z, et al. Research progress on characterizing chemical composition of smokeless tobacco products[J]. Tobacco Science & Technology, 2018,51(2):95-106. [百度学术]
芦 楠,白若石,张 杰,等.不同抽吸方式下改进离子色谱法测定卷烟主流烟气中的氨[J].中国烟草学报,2014,20(4):1-6. [百度学术]
LU N, BAI R S, ZHANG J, et al. Determination of ammonia in mainstream cigarette smoke by improved ion chromatography under different smoking regimes[J]. Acta Tabacaria Sinica,2014,20(4):1-6. [百度学术]
白雪平,黄朝章,张建平,等.卷烟纸特性对卷烟主流烟气中氨含量的影响[J].中国造纸,2010,29(12):27-30. [百度学术]
BAI X P, HUANG C Z, ZHANG J P, et al. Effect of Cigarette Paper on Ammonia Content in Mainstream Smoke[J]. China Pulp & Paper,2010,29(12):27-30. [百度学术]
李 力,戴 亚,李东亮,等.卷烟主流烟气中氨释放量离子色谱测定方法的改进[J].烟草科技,2016,49(4):45-52. [百度学术]
LI L, DAI Y, LI D L,et al. Improvement of ion chromatographic method for determination of ammonia delivery in mainstream cigarette smoke[J].烟草科技,2016,49(4):45-52. [百度学术]
蔡洁云,李雪梅,陈新瑞,等.快速离子色谱法检测卷烟主流烟气中的氨释放量[J].云南化工,2015,42(6):48-52. [百度学术]
CAI J Y, LI X M, CHEN X R, et al. Fast Determination of Ammonia in Mainstream Cigarette Smoke by Ion Chromatography[J]. Yunnan Chemical Technology,2015,42(6):48-52. [百度学术]